骨軟部腫瘍
↓(1)悪性骨腫瘍
↓(2)軟部腫瘍
↓(3)高齢者の悪性骨軟部腫瘍に対する治療方針
↓(4)転移性骨腫瘍
↓(5)自家液体窒素処理骨による再建術
(1)悪性骨腫瘍
悪性骨腫瘍とは骨にできる“がん”のことであり、骨そのものから発生する原発性悪性骨腫瘍と他の癌が転移してくる転移性骨腫瘍に大別されます。
原発性悪性骨腫瘍の種類としては骨肉種・ユーイング肉腫・軟骨肉腫・未分化多形肉腫などがありますが、なかでも最も頻度の高い骨肉種について、金沢大学整形外科で行っている治療も交えながら説明します。
骨肉腫
骨肉腫は骨原発の悪性腫瘍のなかで最も多く、100万人に1~2人の割合で発症し、年間約200人が我が国で発生しています。
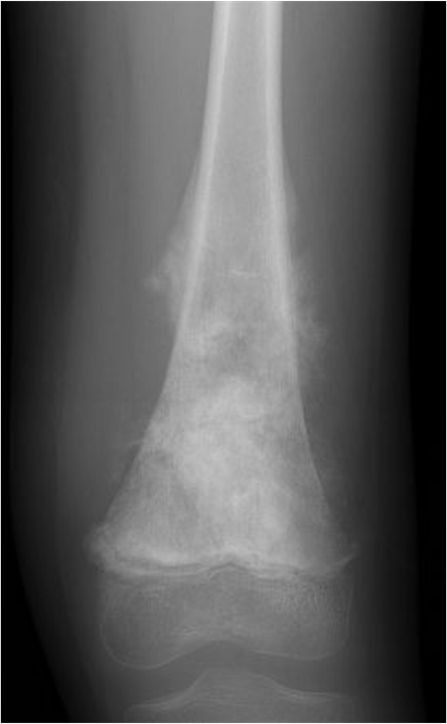
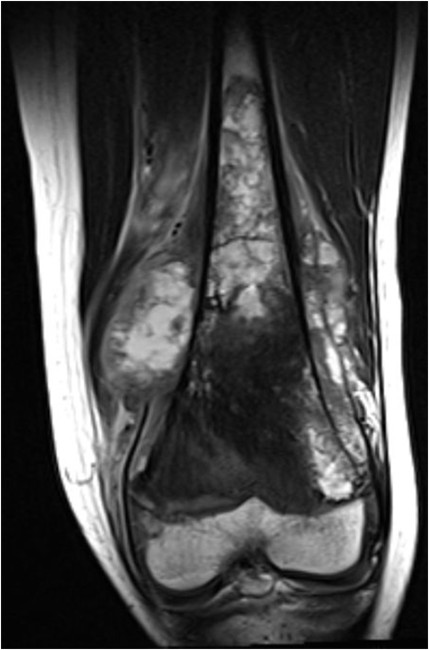
好発年齢は,10代から20代がほとんどで、発生部位は膝関節周辺(大腿骨遠位と脛骨近位)です。他には肩(上腕骨近位)にも多く発生し、これらの部位で全体の約80%を占めます。残念ながら、現在、明らかな原因はわかっていませんが、がんを抑える遺伝子の異常が関与しているという報告もあります。
症状
初発には運動時痛を生じる程度ですが、病気が進行すると安静時痛や夜間痛なども生じてきます。スポーツ活動に伴って痛みを生じることから、筋肉痛などとして放置されることもあり、注意が必要です。骨の外まで腫瘍が大きくなると、外見上腫れてきたり、熱感を生じたりします。時に腫瘍に侵された骨がもろくなり、転倒などを機に骨折を生じて見つかることもあります。
骨肉腫は肺に転移することが多く、病気が進行すると呼吸に障害をきたします。
治療
悪性腫瘍の治療には、現在のところ3つの標準的な治療法があります。手術療法と放射線療法、化学療法(抗がん剤治療)です。骨肉腫の場合には主に化学療法と手術療法が行われます。
1)化学療法
骨肉腫に対しては、1980年代以降から化学療法は必須の治療となっています。化学療法により生存率の劇的な改善が得られました。特に他の癌種と違って、手術前から化学療法を行うことを特徴としています。術前化学療法を行う目的は、以下に示すとおりです。
1. 既に存在している目に見えない微小転移巣(肺,肝,骨など)に対して作用し、転移を撲滅あるいは抑制します。
2. 抗癌剤が有効かどうかを判定し、術後化学療法(手術の後に行うもの)や再発時の化学療法で使用する抗癌剤を選択する場合に利用することができます。
化学療法の多くは、通常3週間程度の間隔をおいて抗がん剤を投与します。これは、1回の抗がん剤による副作用(骨髄抑制,腎臓障害など)から体が回復するために3週間程度の時間を要するためです。
また、術後も化学療法を行いますが、これは手術によって全身に散らばった腫瘍細胞を殺すことや、体内に存在する目に見えない腫瘍細胞を撲滅するために行い、転移や再発の予防につながります。
全体の治療の流れとしては、術前化学療法5コース(5回抗がん剤投与を行う・・・3週×5=15週)、腫瘍切除手術、そして、術後化学療法3~7コース(9週~21週)を行います。したがって、全入院期間は約半年となるわけです。術後の化学療法期間に幅があるのは、全身の状態によって行える化学療法の限度があるからです。

化学療法が行われる以前、すなわち1970年代には20%の生存率であったものが、これらの一連の治療を全て行うことにより、50~70%にまで生存率が改善してきています。化学療法の重要性がご理解いただけると思います。
2)手術療法
骨肉腫の局所治療で最も重要なのは、原発巣の確実な切除です。確実な切除を行うために、各種画像診断を用いて念入りに術前計画をたてます。
手術は切・離断術と患肢温存術とに分けられます。切・離断術は、以前、効果的な化学療法が開発されていなかった時代に多く用いられていた手術法です。患肢温存手術とは、腫瘍を取り残す事なく一塊に切除しながらも、手足を残す手術です。近年、化学療法を中心とした集学的治療の進歩とともに患肢温存手術が標準的な治療法として行われるようになってきました。
治療終了後に肺などへの転移が出現してくることも稀にあるため、退院後も定期的な通院・経過観察が必要です。
(2)軟部腫瘍
軟部組織とは?
皮膚、脂肪などの皮下組織、筋肉、血管、神経、滑膜などの軟らかい組織の総称で、骨や歯、さらに内臓などを除いた組織を指します。
軟部腫瘍の原因
現在のところ、軟部腫瘍の明らかな原因はわかっていません。最近の研究では、ある種の腫瘍では、特異的な遺伝子変異が生じていることが指摘されており、腫瘍の種類によっては、何らかの原因による遺伝変異がその発生の原因ではないかと推測されています。
軟部腫瘍の発生
軟部腫瘍は、全身のあらゆる軟部組織に発生します。痛みを伴わない“しこり”として自覚されることが多く、進行して巨大化するまで病院を受診されないこともあります。患者さんの中には、「痛くないから悪性ではないだろう」と考える方もおられるようですが、腫瘍自体に神経があるわけではありません。腫瘍が神経自体から発生している・炎症物質を産生しやすい・腫瘍が大きくなり周囲の神経などを刺激している、などといった場合を除けば,基本的には悪性腫瘍でも痛みを伴わないことが多いのが実際です。
腫瘍は大別すると良性と悪性(軟部肉腫、あるいは軟部悪性腫瘍といいます)に分けられ、5cm以上の大きさの場合には、悪性の可能性が高くなると言われています。しかし、悪性腫瘍の場合でも、もちろん最初は小さいわけですから、5cm未満の大きさの場合でも、体に腫瘤があることに気がついた場合には、「どうせ脂肪のかたまりだろう」などと放置せずに早めに病院を受診することが大切です。
がんの発生頻度を発生部位別にみてみると、1998年以降肺がんが第1位となっています。それに対して軟部肉腫の発生頻度は、胃がんの1/60、肺がんの1/90とされています、このように軟部肉腫は、肺がんや胃がんなどと比べると発生頻度自体が少ないものです。そのため軟部肉腫の正確な診断や的確な治療に関しては、経験の多い病院を受診することが大切です。良性腫瘍と勘違いされ、誤った切除をされてから、専門施設へ紹介される方も少なからずおられます。軟部腫瘍に関しては、まずは少なくとも専門知識のある整形外科の先生を受診することが大切です。
軟部肉腫の好発部位には、大腿、前腕、上腕、背部などがあります。特に大腿内側(内ももの部分)は、軟部肉腫の好発部位です。この場所はあまり人に見せる部位ではないので、早期の段階で他人から腫瘤を指摘されることはあまりません。人に見られるのも恥ずかしい部位なので、「恥ずかしくて人に見せられない」、とか「病院にかかって悪性と言われるかもしれないので怖い」、といって腫瘍を放置し、腫瘍が巨大化してから「やっぱりどうにもならない」、といって慌てて病院を受診される方もおられます。しかし腫瘍が巨大化するまで放置すれば、転移や手術後の合併症の危険性もそれだけ高まってしまいます。腫瘍が大きくなってから手術を行えば、それだけ切除しなければならない周囲の筋肉の量は多くなり、手術後に重篤な筋力低下などを生じることになります。またこの部位には、下肢全体を栄養している大腿動脈や大腿静脈が存在しており、腫瘍が大きくなると神経・血管が巻き込まれてしまうため、手術が非常に困難となってしまいます。血管を切除し、血行再建術などを行って患肢を切断せず手術を行うことが一般的ですが、それでも手術後には、患肢の腫脹(腫れ)が強く残ってしまうことが多いのが現状です。火事でも,ボヤのうちに火を消すのは比較的簡単ですが、家中大火事になってから火を消し止めるのは、非常に困難です。体にしこりがある方は、そのまま放置せず、一度専門知識のある整形外科の先生に相談してみてください。
軟部腫瘍の組織分類
軟部腫瘍は組織学的に多様で、その種類は良性と悪性をあわせると実に100種類以上あります。そのためときに診断に難渋することがあり、経験豊富な病理医へ診断を問い合わせるため、診断に数週間かかることもあります。主に腫瘍は発生起源をもとにした分類で、脂肪性腫瘍、線維性腫瘍、神経性腫瘍、平滑筋性腫瘍、血管・リンパ管腫瘍などに分けられます。良性腫瘍では、脂肪性腫瘍として脂肪腫、線維性腫瘍として線維腫、神経性腫瘍として神経鞘腫、平滑筋性腫瘍として平滑筋腫、血管・リンパ管腫瘍として血管腫などがあります。悪性腫瘍では、それらの分類に基づいて、平滑筋肉腫、悪性線維性組織球腫、脂肪肉腫、横紋筋肉腫、滑膜肉腫などが頻度の高い腫瘍です。さらに悪性腫瘍は、顕微鏡所見で低悪性度、中等度、高悪性度(悪性度が高いものほど予後は悪くなります)に分類されます。
軟部腫瘍に対する検査
1)血液検査
残念ながら今のところ、軟部腫瘍に対する腫瘍マーカーは見つかっていません。
2)画像検査
軟部腫瘍の画像検査には、レントゲン、CT、MRI、各種核医学検査(PETやタリウムスキャン、場合によっては骨スキャンなど)などが行われます。患者さんによっては、「なんでレントゲンなんて撮るの?」、「MRIだけ撮ればいいんじゃないの?」などと考える方もおられるかも知れません。しかし、血管腫のように特徴的な石灰化を示すような腫瘍や石灰化を生じやすい腫瘍があり、レントゲンやCTでこれらを指摘できれば診断の大きな助けとなります。「MRIを撮れば何でも写る」と思っておられる方がいらっしゃるかもしれませんが、実はCTの方が微細な石灰化を確認するのに適しています。また肺転移のチェックを行うためには、MRIでは撮影に時間がかかり、呼吸の影響で画像がブレてしまうため、CTの方が肺転移のチェックには適しています。このように画像検査には、それぞれ得手不得手があります。また、ここ最近の画像検査の進歩には大きなものがありますが、所詮体の外から“すかして”行った検査ですから、いろいろなアーチファクト(ノイズ)などがまざることも多く、確実に検査を行おうとすると、同じような検査だと思えてもいくつか検査を行い、それらの結果が同じ結果を示していることを確認する必要があります。このことは、軟部腫瘍の場合では単に良悪性のみならず、腫瘍自体の性質で切除の方法などが大きく異なってしまうため、特に重要です。
3)生検術
画像検査で確定診断がつく軟部腫瘍はあまり多くなく、多くの患者さんでは腫瘍の一部を切り取って顕微鏡で腫瘍細胞を確認する生検術が行われることも多いです。「生検術を行うのであれば、画像検査なんてやらなくてもいいのでは?」とおっしゃる患者さんもおられますが、実は腫瘍というのは均一なものではなく、部分部分によっては壊死(死んでいる)を起こし、変性している部分などが混在しています。生検術で腫瘍の診断をつけるためには、その腫瘍の代表的な部分がどこなのかを生検前に知っておくことが重要であり、その意味からも生検術の前に画像検査を行っておくことは重要です。
治療
軟部腫瘍の治療法としては、主に3種類(手術療法、抗がん剤治療、放射線療法)があり、腫瘍の種類や性質により必要に応じて、それらを組み合わせた治療を行います。
1)手術療法
a)良性腫瘍
良性腫瘍で大きさが小さい場合は、経過観察となる場合もありますが、基本的には手術で切除します。これは、上の項でも触れたように、悪性腫瘍でも最初はごく微小な病変から始まるのであり、「5cm以上は悪性を疑わせる」という言葉の裏返しで「じゃあ、5cm未満は良性?」ということにはならないからです。特に病変が小さい場合には、画像検査でもはっきりと病変が写らないこともあり、そのような場合には、切除生検術といって、腫瘍を切除し、標本を顕微鏡で確認して診断をつける必要があります。良性腫瘍だときちんと診断できるのは、標本を顕微鏡で確認して初めてわかることであり、切除したあとの結果論である、ということを認識する必要があります。
転移を起こさない良性腫瘍の中にも、実は局所再発を生じやすいものと生じにくいものとがあります。局所再発を生じにくいような脂肪肉腫や神経鞘腫などの場合には、腫瘍の単純切除(辺縁切除あるいは核出)を行います。しかし、再発を生じやすいデスモイド型線維腫症などの場合では、腫瘍を取り残さないように、一部正常組織をつけて腫瘍を切除することがあります。
b)悪性腫瘍
局所再発や遠隔転移を生じる悪性腫瘍に対しては、腫瘍を取り残さないように切除することが大切で、広範切除(腫瘍を正常組織で取り囲むようにして、正常組織ごと腫瘍を取る)が基本となります。むろん、腫瘍と共に切除する正常組織(通常は筋肉のことが多い)を十分に腫瘍側へ付けることが重要となります。しかし実際には、悪性腫瘍が重要な神経・血管などと接していることも多く、切除縁が腫瘍ぎりぎりとなることも少なくありません。また、切除する筋肉の量が多くなれば、患肢の機能はそれだけ低下していくわけですから、患肢の機能を可能な限り温存するのであれば、できるだけ腫瘍とともに切除する正常組織は少ない方がいいのは言うまでもありません。私たちは悪性度の高い軟部肉腫の場合には、術前と術後に化学療法を行うことで、肺などへの微小転移や局所再発の抑制はもちろん、可能であれば、切除縁を縮小した腫瘍切除を行うことで、患肢機能を温存することを目指して治療を行っています。
2)抗がん剤による化学療法
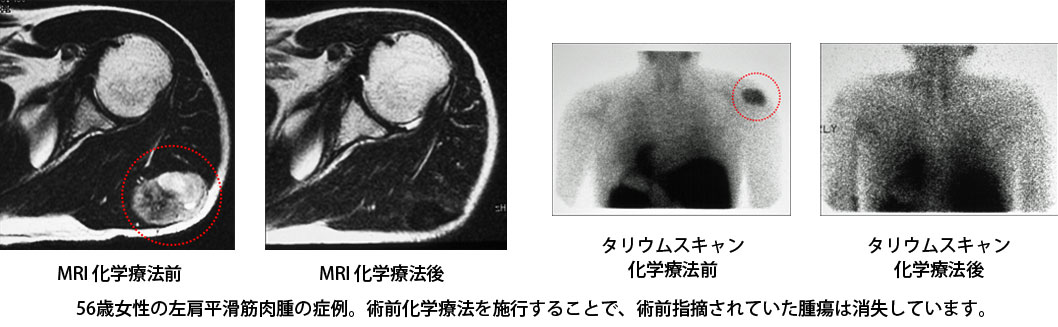
軟部肉腫に対する抗がん剤を用いた化学療法の治療効果に関しては、まだ一定した見解は得られていません。施設によっては、局所の腫瘍を切除するのみで、そのまま治療が終わってしまう施設もあります。しかしこれでは、高悪性度の軟部肉腫の場合などでは、すでに生じているであろう肺などへの微小転移に対しては、何の治療も行えていないことになります。腫瘍の種類にもよりますが、手術単独では、高悪性度軟部腫瘍の約50%の方は、主に肺などへの転移のため数年で亡くなってしまいます。私たちは、高悪性度の軟部肉腫の患者さんに対しても、単に局所の腫瘍を切除するのみで、肺などへの遠隔転移は「運を天に任せて経過を見守る」、というのではなく、可能性のある治療は、できうる限り行っておくことが大切であると考えています。一般的な化学療法の有効率は10~50%程度と報告されています。残念ながら、すべての患者さんで化学療法の効果が得られるわけではありませんが、一部の方では、化学療法の効果が得られているのもまた事実です。治療をしてみなくては、得られるかもしれない治療の効果を得ることは絶対にできません。化学療法は、悪性骨腫瘍のものとほぼ同一の内容で施行しています。症例によっては、薬剤を動脈内投与(カテーテルという細い管を腫瘍の近くの動脈に留置して、持続的に抗がん剤を投与する)します。腫瘍の栄養血管である動脈からすぐに高濃度の抗癌剤が到達するため、腫瘍の縮小効果が期待でき、腫瘍を取り残さずに正常な機能を損なうことを最小限とした手術を行える可能性があります。動脈内から点滴された抗癌剤はその後、静脈を通過して全身に循環します。そのため画像にはうつらない肺や他の骨の微小転移巣に対しても抗癌剤が効果的に作用することが期待できます。
3)放射線照射
軟部肉腫に対する放射線照射に治療効果に関しては、まだ一定した見解は得られていません。しかし腫瘍が手術でしっかりとは取りきれない時などには、放射線の照射を行うことがあります。患部への放射線の照射は、手術前に行う施設と、手術後に行う施設があります。手術前に放射線照射を行うと、皮膚や軟部組織障害により、手術時の合併症が増加することがあり、当科では、神経や血管に軟部肉腫が接していたり、腫瘍が一部分取りきれなかった場合などに、必要に応じて放射線の照射を行うこととしています。
(3)高齢者の悪性骨軟部腫瘍に対する治療方針
高齢者と呼ばれている方の中にも、「私はまだ若いしピンピンしている、まだまだ高齢者などと呼ばれるような年齢ではない」などと思っている方も多くいらっしゃるのではないかと思います。「高齢者」といっても、各種統計の取り方によりその年齢はまちまちですが、世界保健機構(WHO)の基準に従い65才以上の方を高齢者としている場合が多いようです。
1935年(昭和10年)の日本人平均寿命は男女とも50年もありませんでしたが、2007年(平成19年)の時点で、いまや男性平均寿命は79.2才、女性平均寿命は86.0才となっています。日本は世界的にみても最も高齢化率の高い国の一つですが、このような日本人の高齢化と共に、高齢者の方の悪性骨軟部腫瘍の発生頻度は年々上昇してきています。

高齢者の悪性骨軟部腫瘍の患者さんの中には、「高齢者になったのだから」と積極的な治療をあきらめてしまう方がいらっしゃいますが、65歳で発症したとしても、「がん」を克服することができればまだ残りの人生は20年ほどあるのであり、まだまだ人生をあきらめてしまう年齢ではありません。

いわゆる高齢者の方の悪性骨軟部腫瘍に対する治療方針については、各治療施設ごとにバラバラであり、施設によっては特に全身状態に問題がなくとも、単に65才を超えたというだけで抗がん剤を使った治療を行わない、といった施設もあります。しかし、私たちは、「がん」という命に関わる病気を相手に戦うためには、単なる目に見える手足の病巣を手術で切除するだけではなく、有効な可能性がある治療法は積極的に併用して治療にあたる必要があると考えています。例えば局所の腫瘍を切除するだけでは、悪性細胞の全身への転移に対しては全くの無効であり、肺などへの転移に対しては運を天に任せて経過をみるしかありません。
私たちは、単に年齢だけで抗がん剤を用いた治療の適応の有無を決定するのではなく、患者さんの個人個人において抗がん剤を用いた治療が施行可能かを判断し、施行可能な場合には積極的に抗がん剤を用いた治療を行っていく必要があると考えています。また、抗がん剤が有効で腫瘍が縮小した場合には、患肢の機能を可能な限り温存することも可能となります。45歳を過ぎると年間2%程度の筋力が自然と失われていくといわれています。下肢筋力の低下は、転倒、寝たきりなどの大きな原因の一つであり、高齢者といえども縮小手術で神経・血管などとともに筋肉を温存することには大きな意義があるといえます。
以上のように、抗がん剤による治療が有効であれば患者さん自身が得られるメリットは極めて大きいものとなるのですが、残念ながら現在のところ、抗がん剤がその患者さんに有効かどうかということは、実際に患者さんに抗がん剤を投与してみないとはっきりとはわかりません。そこで私たちは、入院時の検査で全身状態が大きく低下していないような高齢者の方の場合には、若い患者さんで用いる7割程度の抗がん剤の量から投与を開始し、全身における副作用出現の程度、腫瘍に対する化学療法の効果を判定しながら、抗がん剤を使った治療を継続するべきか判断しています。
また、残念ながら抗がん剤の副作用が強く出てしまう方や、抗がん剤の無効な方など、抗がん剤による治療が行えないような高齢者の方などには、免疫療法による治療なども考慮して治療にあたっています。
(4)転移性骨腫瘍(主に上肢・下肢)
転移性骨腫瘍とは?
転移性骨腫瘍とは、癌が骨に転移したもの(骨転移)で、どの癌にも骨転移を起こす可能性があります。特に頻度の高いものには、肺癌、乳癌、前立腺癌、腎癌などがあります。原発巣に対する有効な治療方法が増え、癌の患者さんが長く生きられるようになった半面、転移性骨病変を有する癌患者さんは増加しており、骨への転移による痛みや骨折、脊椎(背骨の骨)への転移による麻痺のために、何らかの治療を要する患者さんはむしろ増加しているのが現状です。骨への転移のため骨折を起こした場合や、脊椎(背骨)の転移のため神経麻痺が出現した場合などは、緊急に手術を要することがあります。
症状
転移した腫瘍がまだ小さく、周囲の骨を壊すことなく骨の中にとどまっている場合には、痛みなどの症状はほとんどありません。腫瘍が大きくなり骨の破壊が進んだ不全骨折という状態になると、安静時にはあまり症状はありませんが、体重をかけた際などの運動時に痛みが出現するまでになります。さらに腫瘍が大きくなり骨の大部分が腫瘍に侵されると、軽い外傷で骨折を起こすようになります。また脊椎に転移し骨がつぶれて脊椎の圧迫骨折などを生じた場合には、腰痛や背部痛となって痛みを感じます。また脊椎に囲まれた脊髄神経が腫瘍で圧迫されると、手足のしびれや麻痺が出現します。
診断
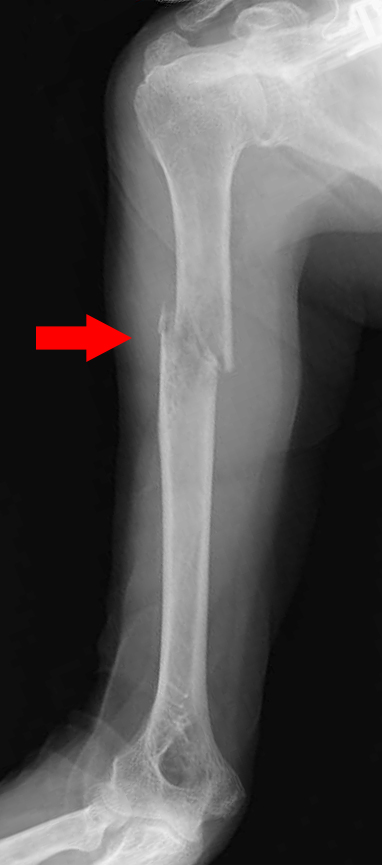
転移性骨腫瘍がある場合には、レントゲンで骨が溶けてきている、白くなってきている、潰れてきているといった所見がみられることがあります(図の矢印)。またMRIでは、レントゲンで指摘できないような初期の段階の転移や、骨髄内の病変の広がり、病巣の性状などがより詳しくわかります。脊椎の場合には、神経の圧迫の状態もわかります。核医学検査である骨シンチグラム、タリウムシンチグラム、PETスキャンなどは、一度に全身を撮影できるので、全身のチェックを行うのに有用です。また血液検査では、原疾患の腫瘍マーカー、吸収マーカー、血清カルシウム値の確認などが骨転移の診断に有用な場合があります。原疾患の担当医と、各検査の内容や施行するタイミングなどを相談する必要があります。
治療
むろん原発巣の治療が優先ですが、転移性骨病変による痛みや骨折は、患者さんの日常生活の質(QOL)を大きく低下させてしまうため、原発巣の治療と平行して治療を行っていく必要があります。
1)薬物治療
最近の劇的な進歩のひとつに、ビスフォスフォネート製剤の開発があります。ビスフォスフォネートの注射薬を月1回程度点滴投与することで、癌による骨関連事象(骨転移巣の形成や骨転移による骨の痛みなど)の出現を低下させることができます。抗癌剤とは異なり、それほど大きな副作用もありません。その他にも痛みに対して、鎮痛剤やモルヒネなどの麻薬を用いることがあります。
2)放射線治療
放射線をあてることで、癌細胞を殺します。癌の種類によって効果は様々で、癌の治療目的や、除痛目的のために放射線を照射します。一般的には、放射線照射は外来に通院しながら施行することが可能です。放射線照射により、皮膚障害や内臓などの臓器障害が出現することがあり、照射の部位や回数については、放射線治療の専門医と十分に相談することが大切です。
3)手術治療
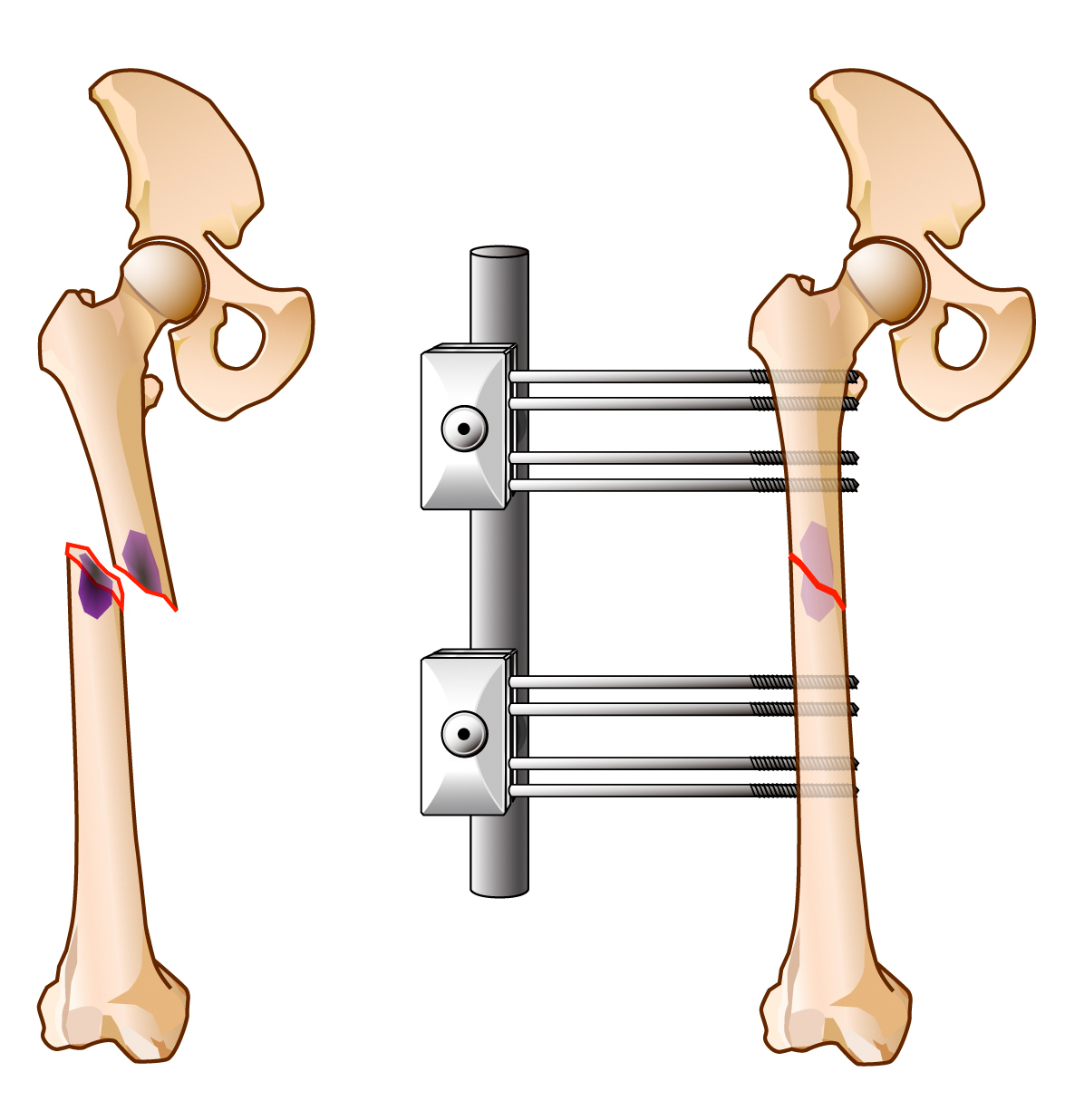
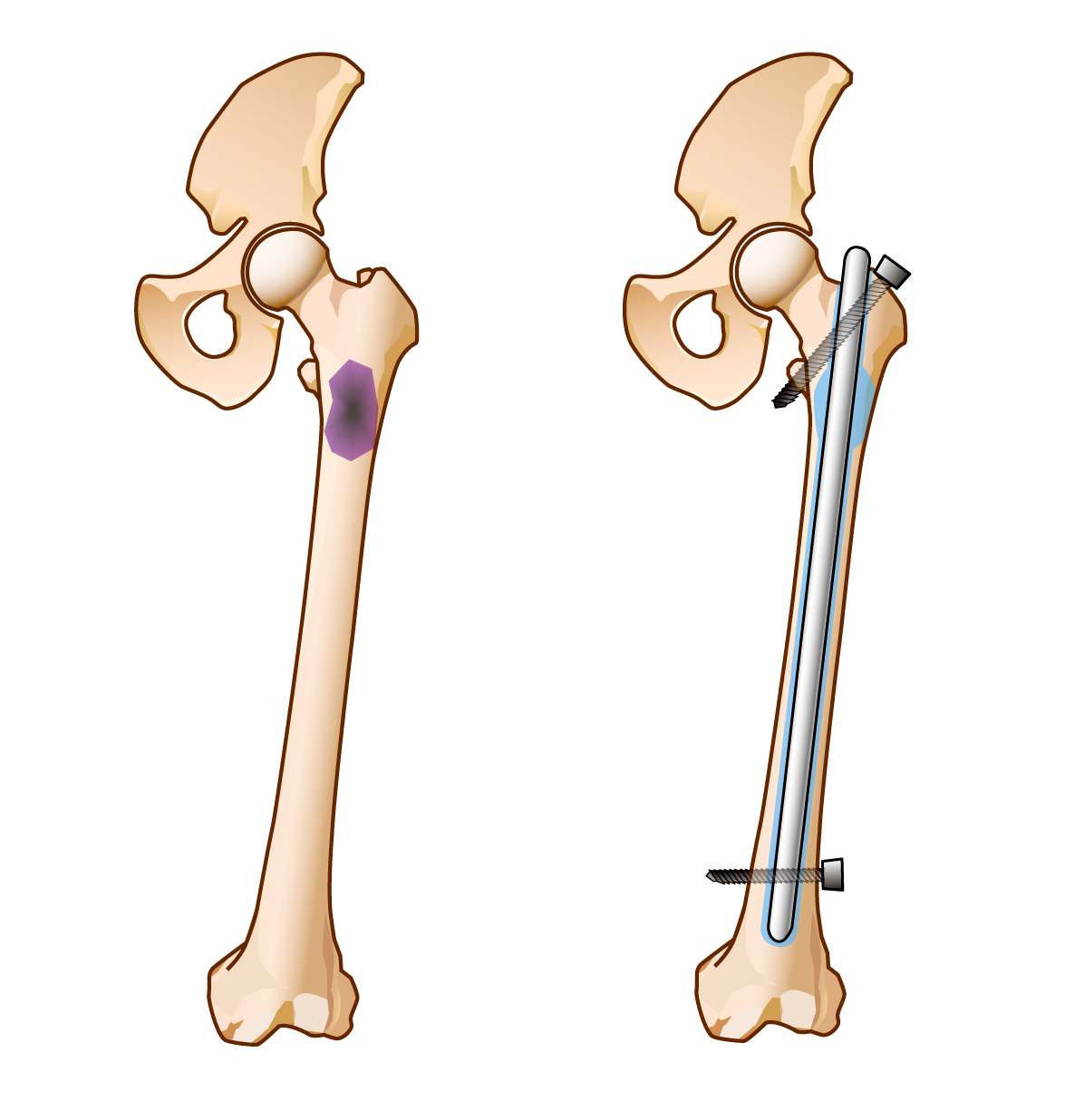
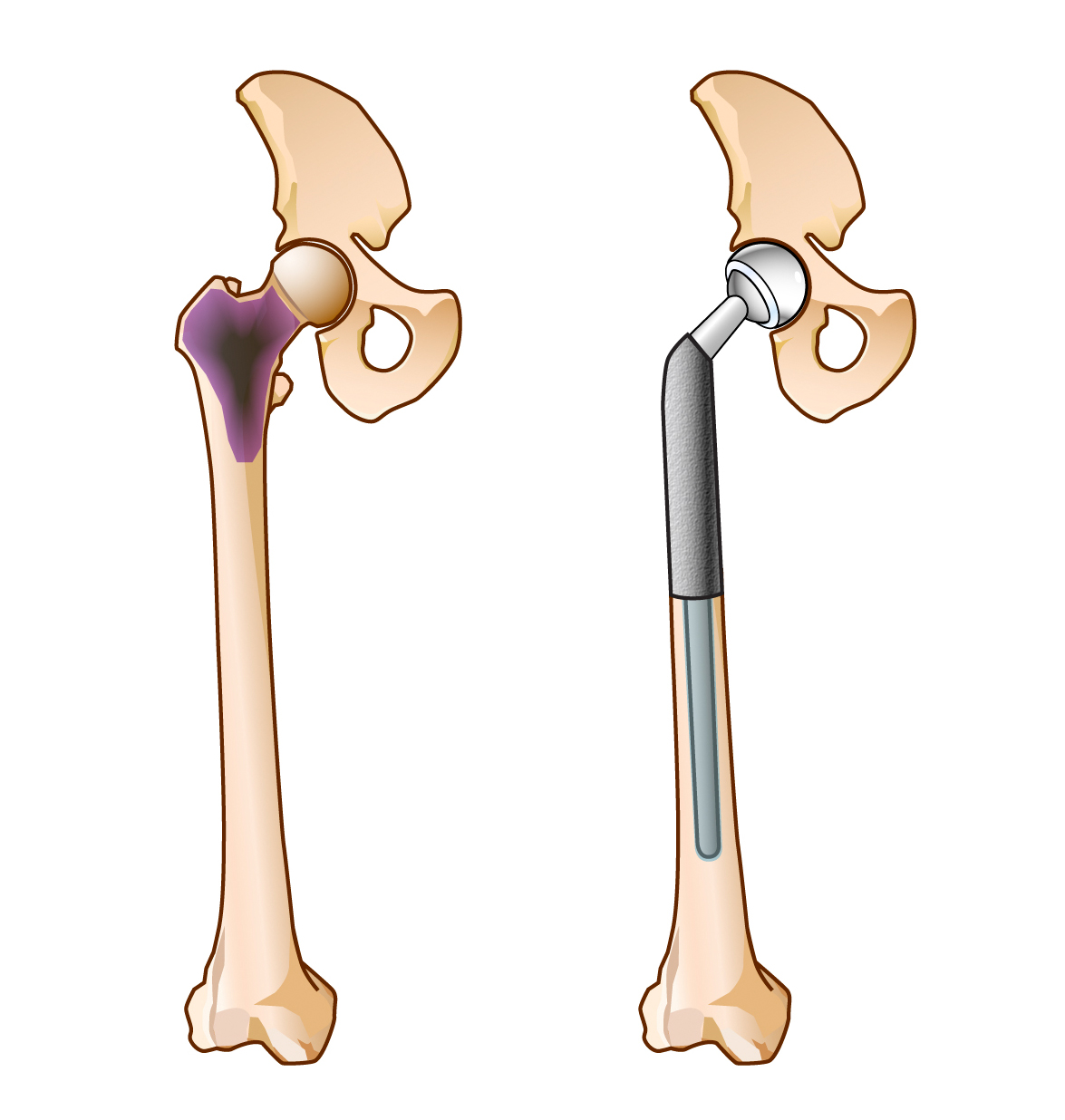
手術方法は、患者さんの全身状態や予後などを総合的に判断して決定しています。具体的には、四肢の転移性骨腫瘍の場合、患者さんの全身状態が悪く、予後もあまり期待できない患者さんでは、創外固定器を用いた骨折部の固定を行います。また予後が半年程度と見込まれているような患者さんでは、早期社会復帰を考え、腫瘍部位へ骨セメントなどを充填し、髄内釘やプレートなどの金属で骨折部を固定する手術を行います。また予後がより長期間見込めるような患者さんでは、局所の根治を考え、腫瘍の十分な切除と腫瘍用人工関節を用いた再建術を行います。むろんそれぞれの手術方法には長所や短所があるため、手術を行う整形外科医とよく相談して手術方法を決める必要があります。
非常に重要なことは、麻薬の服用や放射線の照射では、骨転移による痛みが楽になることはあっても、骨の強度が十分に回復することはないということです。痛みを取り除き、骨の強度を十分に回復することができるのは、手術だけです。
癌の骨転移というと癌の末期と捉えられ、お医者さんの中にも、骨折を起こさない限りは「いまさら手術など行わなくても」と考えられる方がおられます。しかし、「いつ折れるかわからない」という不安の中で生活をしたり、「骨折をする可能性が高いから足をついたらダメ。車椅子で生活するように。」といった、自分の大切な最後の時間に生活が大きく制限されてしまうような状態は、患者さんにとって大変不幸なことです。私たちは、最後のときまで、自分の行きたい所へ、自分の好きな時に、自分の力で歩いていけるということは、非常に大切なことであると考えています。手術を行うことで、最後のときまで充実した生活が送れるよう、私たちは、手術が必要な患者さんに対しては、積極的に手術を行うようにしています。
(5)自家液体窒素処理骨による再建術
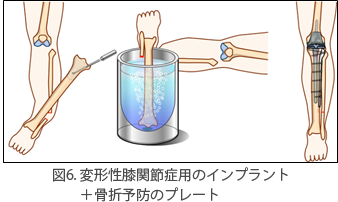
悪性骨腫瘍(がんの骨転移を含む)を手術で切除した場合,切除した骨の部分(骨欠損部)をどのように再建するかという問題が生まれます.腫瘍用に作られた大きな人工関節(腫瘍用人工関節,図1)を用いれば,大きな骨欠損も補うことができますが,非生体材料(金属やポリエチレンなど)を用いた再建であるため,中長期的にみると,人工関節が摩耗し,緩んだり,折損したりすることが問題となります.
また腫瘍用人工関節を用いた場合,腫瘍が関節に及んでいなくても,正常な関節(軟骨や靭帯など)も一緒に切除することになり,術前と比べて膝関節の機能が大きく低下することが一般的です.
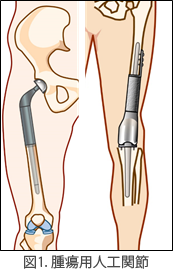
このような問題を解決するために,金沢大学整形外科では,腫瘍とともに切除した骨を一塊として液体窒素の中で処理し,腫瘍細胞を死滅させたうえで再び体に戻して骨欠損部を再建する方法を考案し,基礎実験に基づいて,1999年から臨床応用してきました.2004年からは先進医療として治療を行い,2020年4月から処理骨自家骨移植の一つとして保険承認されました.
液体窒素処理骨では,処理直後の力学的強度が処理前と同等に保たれることや,凍結免疫(液体窒素で処理した細胞が体の腫瘍に対する免疫力を高めること)を期待できることなど,悪性骨腫瘍の治療に有利となる特徴を多く有していることをこれまでの研究で明らかにしてきました.
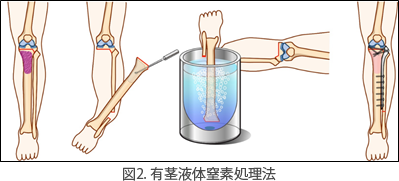
私たちはこの治療を応用して様々な再建方法を考案し,患者の皆さん一人一人にとってベストとなる治療法を選択しています.液体窒素処理した骨が早く回復し,少しでも早く生活に復帰できるために,大腿骨や脛骨などの近位(体の中心側)にある骨腫瘍では,腫瘍部を体から切り離すことなく液体窒素処理する方法(有茎液体窒素処理)を行っています(図2).
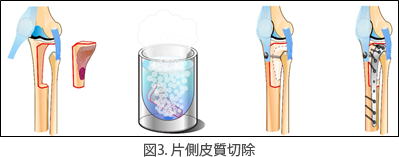
化学療法が効果的な場合,対側の骨を温存して腫瘍を切除し,再建を行うことでも,処理骨のより早い回復を期待することができます(図3).
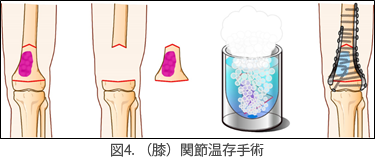
化学療法が効果的で腫瘍が関節に及んでいない場合では,関節を温存するように腫瘍骨を切除し,液体窒素処理骨再建を行うことで,より良好な機能温存を行うことができ,術前と同じように生活し,スポーツに復帰した方も多くいます(図4).
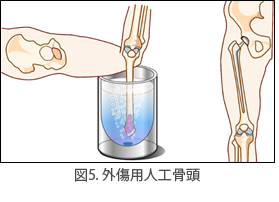
腫瘍が関節に及んでいる場合でも,液体窒素処理後に関節面のみ通常の人工関節に置換し,靭帯などを再建(処理骨に再縫着)することで,腫瘍用人工関節に比べて,良好な機能を得られます(図5, 6).
これまで,金沢大学整形外科では,悪性骨腫瘍の治療において,液体窒素処理骨による再建術を150人以上の方に行い,良好な長期成績を収めています.
(6)新たな治療法:経皮的ラジオ波焼灼(RFA)
経皮的ラジオ波焼灼療法(Radiofrequency ablation: RFA)は,CTなどの画像を見ながら電極針を病変部に刺し,高周波電流を用いて腫瘍の異常細胞を焼灼する治療法です.もともとは肝臓の腫瘍に対する治療として保険適用となっていましたが,2022年9月に肺悪性腫瘍,小径腎腫瘍,悪性骨腫瘍,骨盤内悪性腫瘍,四肢・胸腔内及び腹腔内に生じた軟部腫瘍,類骨骨腫(良性骨腫瘍)に対して保険適用が拡大され,整形外科領域でも広く行われる治療になっています.
RFAは,電極針を刺すための小さな切開のみで治療が可能なため,身体への負担が少ない低侵襲な治療法です.さらに,病変部をピンポイントで治療可能なため,近接する臓器機能を温存できるなど,様々な利点があります.
今回の保険適用の拡大に伴う整形外科領域での主な対象疾患は,転移性骨腫瘍(がんの骨転移病変),良性骨腫瘍である類骨骨腫,骨盤内悪性腫瘍になります.
特に近年,類骨骨腫に対するRFA療法が注目されています.良性骨腫瘍である類骨骨腫は小児の四肢の骨に好発し,多くの症例で夜間に増強する強い疼痛を伴います.内服薬が奏功する場合もありますが,改善が得られない場合は手術での骨腫瘍切除を行います.手術では病変周囲の正常な骨も同時に切除せざるを得ない場合があり,侵襲が大きくなり術後に骨折をきたす可能性があります.一方,RFA療法はCTを見ながら確実に病変部を焼灼することが可能であり,低侵襲で除痛効果に非常に優れた治療法として,良好な治療成績の報告が散見されます.
当科では,麻酔科,放射線科と協力し,類骨骨腫に対しては数日の入院で治療を行っています.転移性骨腫瘍や骨盤内悪性腫瘍においては,原発科と治療方針を相談して入院治療を行っています.
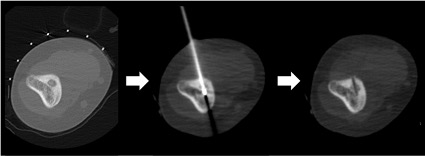
(図)CT画像を見ながら電極針が病変部に確実に刺さっていることを確認後,高周波電流を流すことで病変部の腫瘍細胞を焼灼します.